前言:受新冠疫情的影響,2021年醫療器械和IVD行業在面對巨大挑戰的同時,繼續保持穩步增長,其產品的生產也離不開受控潔凈區,現分享潔凈區的關鍵潔凈度指標——塵埃粒子等相關法規。
《醫療器械生產質量管理規范附錄無菌醫療器械》描述:“2.7.3 應當按照醫療器械相關行業標準要求對潔凈室(區)的塵粒、浮游菌或沉降菌、換氣次數或風速、靜壓差、溫度和相對濕度進行定期檢(監)測,并保存檢(監)測記錄。”
1、合格標準
靜態數據參考《醫療器械生產質量管理規范》
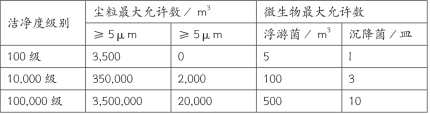
動態數據建議參考制藥GMP
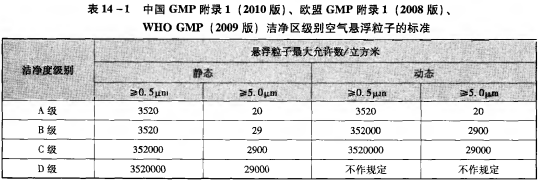
2、定期監測頻率
靜態監測參考《GB 50457-2008 醫藥工業潔凈廠房設計規范》、《GB 50591-2010 潔凈室施工及驗收規范》,對于ISO1-5級區域,空氣潔凈度監測周期不長于6個月,對于ISO6-9級區域,不長于12個月。
動態監測根據用戶實際情況和風險評估而定,或參考《2010年藥品GMP指南:無菌藥品》,百級每批一次,萬級、十萬級每月一次。
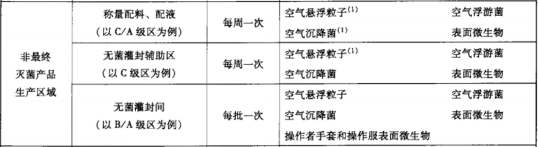
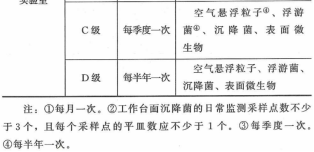
實驗室參考:《GBT 14233.2-2005 醫用輸液、輸血、注射器具檢驗方法 第2部分:生物試驗方法》指向最新版中國藥典《1101無菌檢查法》,《1101無菌檢查法》指向《GBT 16292:2010醫藥工業潔凈室(區)懸浮粒子的測試方法》和《9205 藥品潔凈實驗室微生物監測和控制指導原則》,百級每季度一次,萬級和十萬級每半年一次。
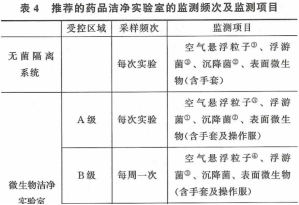
問題:是否計算房間UCL結果?
回答:按照《GB 50457-2008 醫藥工業潔凈廠房設計規范》要求,粒子監測參考《GBT 16292:2010 醫藥工業潔凈室(區)懸浮粒子的測試方法》,級別為百級、萬級、十萬級,生產或檢測區域潔凈度不低于十萬級。GBT 16292:2010是參考最新版的《ISO 14644-1:2015 潔凈室和相關受控環境 第一部分:根據粒子濃度劃分空氣潔凈度等級》,現最新版為2015版,取消計算房間UCL。
推薦使用TSI 9500系統便攜式粒子計數器,適合醫療器械、IVD和制藥行業的塵埃粒子監測。
1、有28.3L、50L、100L型號,適用于不同潔凈級別百級、萬級、十萬級或ABCD級潔凈區的采樣量要求。
2、內含多種標準ISO14644-1:1999、EUGMP-ISO:1999、ISO14644-1:2015、EUGMP-ISO:2015,適合醫療器械、IVD和制藥行業的新版和舊版法規塵埃粒子監測,含95%UCL計算。
3、通過輸入面積、潔凈等級、選擇標準和房間狀態后自動生成通道、取樣量、位點數、取樣時間等的數據,其數據完整性符合FDA 21 CFR PART11、Part211和212要求。自動化、操作簡便。
